PE Expert D course 概要
2025年2月より後継プログラムへ移行中
SMDとは?
Specialist in Medicines Developmentの略称です。
SMDプログラムは、医薬品の開発に始まり市場における適正使用を導く製薬医学について普及啓発するNPO法人国際製薬医学会(IFAPP :International Federation of Associations of Pharmaceutical Physicians and Pharmaceutical Medicine)と、各国の製薬医学教育コースを認証するヨーロッパのNPO法人PharmaTrainによる合同プロジェクトとして、2016年に開始されました。
従来の教育コースのような座学を主とした基礎知識の習得とは異なり、本プログラムでは、参加者の職場における実務遂行能力(コンピテンシー)の評価と育成を行います。その結果、IFAPPとPharmaTrainが定める国際的カリキュラムの基準に達した個人に対して認定が発行されます。
SMDプログラムの背景
創薬技術の革新による難病治療薬の開発や、医療機器とのコンビネーション、再生医療への展開が注目される中で、医薬品の研究開発や診療現場との橋渡しで活躍する医薬品開発専門家へのニーズが国際的に高まりつつあります。一方で、多くの職場では体系的な教育カリキュラムや評価基準が確立しておらず、優れたコンピテンシーを持つ人材を識別して計画的に育成することは容易ではありません。知識だけではなく行動による具体的な成果が求められるビジネスにおいては、客観的な能力評価と効果的な人材育成がますます重要となっています。
そこで、2016年にヨーロッパと日本でパイロットプロジェクトを実施することになり、日本では(一財)日本製薬医学会、(一社)日本ACRPおよび欧州製薬団体連合会が(一社)日本臨床薬理学会の後援のもとに合同で参加しました(ヨーロッパではイタリアが同時に導入開始)。試行的導入を経て、2020年8月からは当法人で運用を開始しており、引き続き(一財)日本製薬医学会、(一社)日本 ACRP、欧州製薬団体連合会の後援を受けています。
特に、日本製薬医学会と大阪大学の 新PharmaTrain教育コース の受講修了者には、職場でのコンピテンシー評価を得ることでSMD認定の取得が期待されます。
WATCH VIDEO
 [2021年4月26日] WATCH VIDEO
[2021年4月26日] WATCH VIDEO
SMDプログラム(Dコース)座談会
SMDプログラム(Dコース)の参加者とメンター、レビューワーが大集合で座談会を開催しました...
D.開発専門家コース(SMD認定):業界・アカデミア向 (2020年10月開講) * 2025年2月より後継プログラムへ移行中
- 目 的:職場でのコンピテンシー育成と評価
- 対 象:主に業界やアカデミアで研究開発に関わる人、または学習を希望する人
- 人 数:20人程度(最大40人まで)
- 日 時:2020年10月開講
- 回 数:定期評価(3ヶ月毎) +年次第三者評価
- 参加費:(一社)医療開発基盤研究所の会員(個人及び法人賛助社員)には割引があります。
受講種別* 年間参加費(税込) メンター委託費(税込:年間参加費に追加) 法人研修としての受講 47,143 55,000 個人としての受講(所属する法人からの参加費支援が無い場合) 33,000 38,500
*法人とは受講者の所属機関(企業・大学・医療機関等)のことです。
SMD Competency Domain List
| SMDコンピテンシーのドメインリスト | ||
|---|---|---|
| Domain 1 | Discovery medicine & early development | アンメットメディカルニーズの把握、新規開発候補の評価とTarget Product Profile作成に向けた臨床開発をデザイン化する |
| Domain 2 | Clinical development & clinical trials | 探索・検証臨床試験を企画・実施・評価し、論文発表や薬事申請文書を作成する |
| Domain 3 | Medicines Regulation | 医薬品のライフサイクルを通しての適正使用とリスク管理のための臨床開発に必要な薬事・法制度を理解する |
| Domain 4 | Drug safety surveillance | 患者と被験者に適切な情報を提供し、リスクを最小化するための市販後サーベイランスを評価・解釈する |
| Domain 5 | Ethics and subject protection | 臨床試験の実施とコマーシャル活動における臨床試験倫理とビジネス倫理の基本を理解し、行動する |
| Domain 6 | Healthcare Marketplace | 医薬品のプロモーションや臨床試験の企画において被験者保護に必要な倫理・法的基準を理解し、行動する |
| Domain 7 | Communication & management | 効果的なコミュニケーションスキルや対人関係構築で成果達成に必要な人材管理やリーダーシップを発揮する |
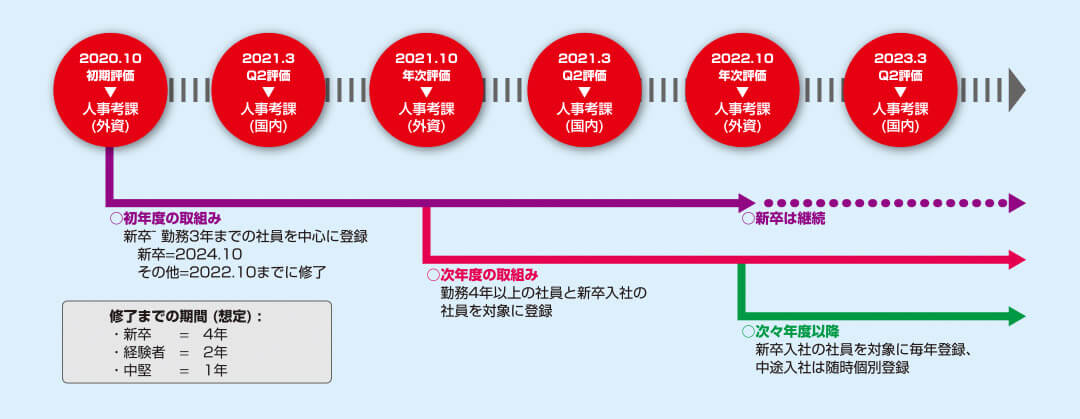
グループでの参加(例)
SMDプログラムをグループ(職場単位)で申し込む場合、対象となる職員の経験年数に合わせたグループ参加が考えられます。
下記の図は企業での人事評価時期に合わせた一例で、参加企業の年間スケジュールに連動することでSMDプログラムでの評価結果を人事評価に取り入れることができます。年度の開始月は相談に応じます。